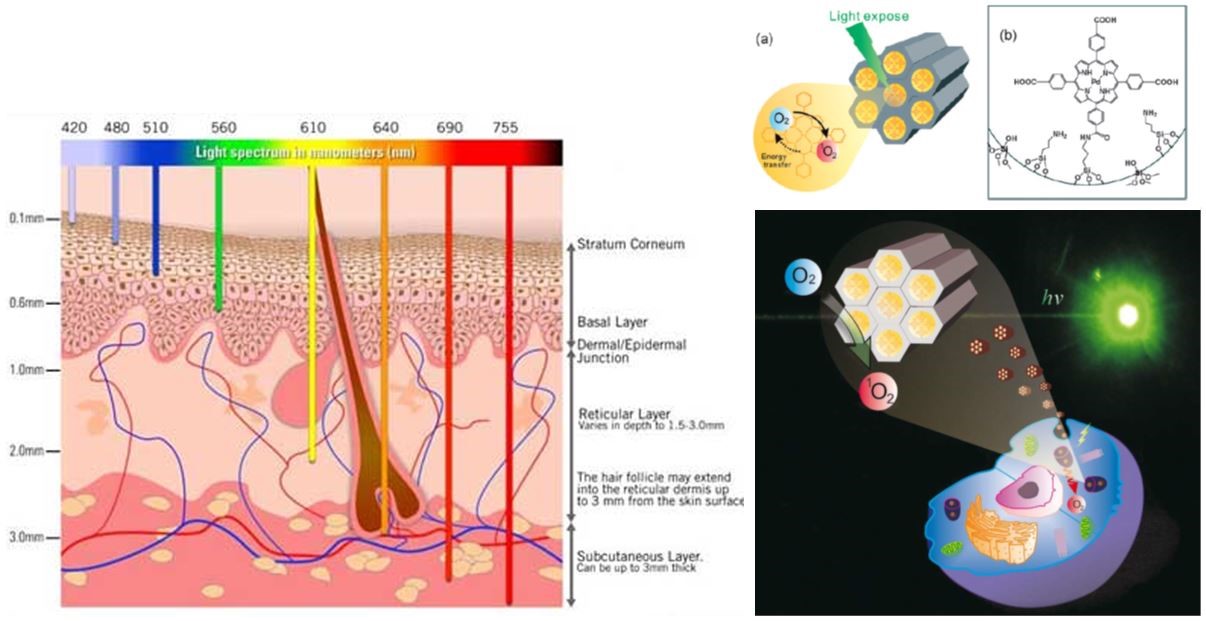
單光子近紅外光源具有絕佳的生物體穿透性質(約700~1000奈米),應用於淺層腫瘤的治療上,可避免血液及組織等內源性物質的干擾。本所羅履維研究員團隊早期運用中孔洞奈米矽球(Mesoporous silica nanoparticles,MSNs)附載光敏劑Pd-porphyrins,設計出新式奈米光動力平台。於此平台下,MSN–PdTPP同時具備影像診斷及治療雙重功能,於癌症的診斷治療上,提供一新的方向。
中期研究方向-- Two photon activated photodynamic nanotherapy and the real-time imaging of its bioelimination in vivo
雙光子技術的應用除強化表層診療之穿透性(可達數百微米)外,其影像解析度更優於單光子雷射技術。本所羅履維研究員團隊以MSN作為奈米載體,以MSN骨架內的FITC作為天線吸收近紅外光能量,同時將能量傳遞給孔洞內之光敏劑來執行光動力治療。羅履維研究員團隊利用此雙光子技術動態追蹤奈米載體於活體內的代謝情況。於本研究中證實奈米粒子之表面電性與肝臟細胞間具有顯著關聯。此發現可作為未來藥物設計之參考依據,同時亦有助於引領後續奈米藥物之設計,以減緩藥物的肝毒性及加速藥物在肝臟清除之效能。
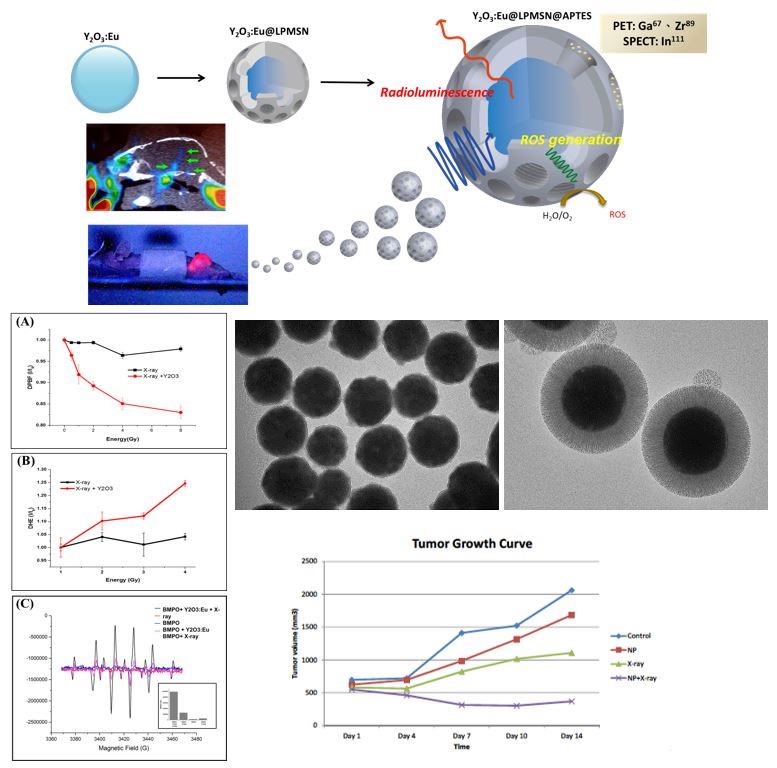
現今研究方向-- X-ray responsive nanoscintillators for multifunctional cancer theranostics
X-ray提供一非侵略式之診療選擇。本所羅履維研究員團隊應用MSN結合Yttrium oxide開發出另一新型的多功能奈米診療平台。此平台可應用於深層非侵入式診斷治療(達數十公分)。於此研究中,羅履維研究員團隊先後以此奈米載體以單光子電腦斷層掃描攝影術(single photon emission computed tomography,SPECT)觀察神經幹細胞的移轉,同時透過radioluminescence特性,即時追踪治療之情況。近年來我們亦證實此多功能奈米載體在吸收x-ray能量後可轉換成活性氧化物質(reactive oxygen species,ROS)。此搭配x-ray之PDT診療平台,不但能克服傳統PDT對深層組織應用之限制,亦可改善其對氧分子之依賴性,大大的提升治療的效果。