社團法人國家生技醫療產業策進會為鼓勵我國產業創新與研發,自2004年起設立「國家新創獎」,並依對象分為「企業新創獎」、「學研新創獎」與「臨床新創獎」等獎項。本院生醫工程與奈米醫學研究所林淑宜副研究員獲該會邀請以「於腫瘤細胞活化的鉑金藥物」研究參賽,並以其卓越成果榮獲第12屆學研創新獎。林淑宜副研究員2011年時便曾與本院楊重熙特聘研究員及中央研究院胡宇光研究員共同獲得第8屆學研新創獎,本屆再獲肯定,本院與有榮焉。
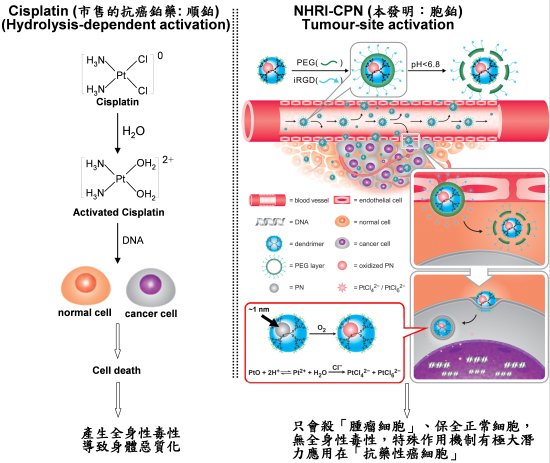
本屆獲評審青睞的「於腫瘤細胞活化的鉑金藥物」研究,其創新特色在於林副研究員發展出一種具有「於腫瘤細胞始活化」專一性的新型奈米鉑金藥物—「胞鉑」(NHRI-CPN,英文為bubble-platin)。目前治療惡性腫瘤的化學療法中,半數以上會使用含有成分為「鉑金」的藥物,其中最為有名的是「順鉑(cisplatin)」。此類藥物會因被水解產生毒性以抑制癌細胞,但缺點是也會毒害健康細胞,造成嚴重的副作用或身體惡質化現象。林副研究員發展出的「胞鉑」藥物,其關鍵原理是利用新穎合成方式,提供約大小1 nm的奈米鉑(大約由35顆鉑原子組成),其結構因約有90%的鉑原子暴露於奈米鉑表面,可增加鉑原子和氧氣接觸的機會,形成可溶解的「氧化奈米鉑」,並於合成時特別包覆一層對酸性敏感的聚乙烯組(polyethylene group)(例如聚乙二醇(polytheylene glycol, PEG)。該藥物經由胞吞作用被細胞吞噬後,會因癌細胞中弱酸且含氯離子的環境先使PEG剝離,內層的奈米鉑金藥物再經內嗜作用進入細胞溶小體,並釋出有毒的鉑離子。最後,鉑離子會嵌入細胞核內的DNA,導致癌細胞無法複製而凋亡(圖一)。這個「於腫瘤細胞始活化」的致死機制卻不影響正常細胞生理狀態,故可大幅減輕患者的身體負擔。這創新的想法亦獲得科技部生技醫藥國家型科技計畫的經費支持。
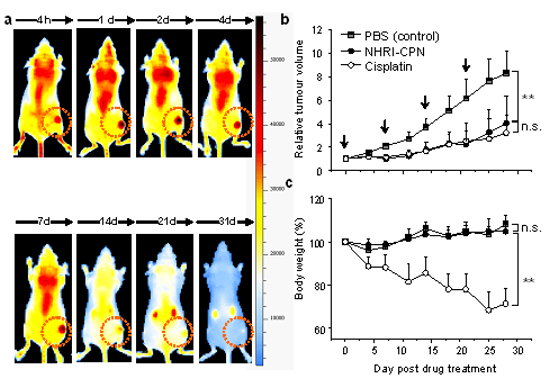
從動物實驗成果中顯示,使用「順鉑(cisplatin)」的老鼠在腫瘤變小的同時,食慾下降,體重也大幅減輕;而使用「胞鉑」藥物的老鼠,其腫瘤雖變小,體重非但沒有下降,食量反而增加(圖二),證實本藥物不會產生全身性的毒性或身體惡質化的現象;同時,驗證其肝腎功能後也發現沒有產生毒性或病變,並可排出體外。另在細胞與動物實驗成果中,更發現「胞鉑」藥物對具三陰性乳癌(MDA-MB-231)具有特別療效,此研究成果獲國際知名期刊Advanced Materials (2013;25: 5067-5073)肯定。近期的研究數據也顯示,此新藥對於有抗藥性的患者在肺腺癌上皮細胞(A549cis)其毒殺的效果也相當卓越。未來希望攜手國內廠商於完成臨床試驗等法定規範後,投入目前達上百億美金規模的癌症用藥市場。